1. INTRODUCCIÓN
El Comité Técnico 209 de ISO ha estado trabajando desde el año 2010 en una revisión de las normas ISO 14644-1:1999 y ISO 14644-2:2000 que son las normas que marcan la clasificación y controles a realizar en las salas limpias, tras un proceso de revisión largo finalmente en Diciembre 2015 ha salido el documento definitivo.
En este artículo nos centraremos en los cambios de la primera norma en general y en los límites y tamaños de partículas en función de la clase. En próximos artículos analizaremos los demás cambios de esta normativa.
2. ¿QUÉ CAMBIA EN LA ISO 14644-1-2015?
En la edición de 2015 hay tres grandes cambios respecto a la edición de 1999:
– Límites de concentración de partículas en función de la clase y el tamaño de partícula.
– El sistema para determinar el número mínimo de localizaciones a muestrear.
– El criterio de aceptación para la determinación final de la clase.
3. CAMBIO EN LOS LÍMITES DE CONCENTRACIÓN DE PARTICULAS
3.1 Límites
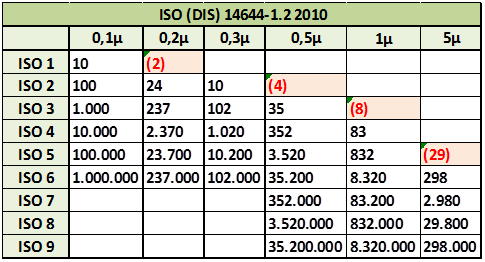
Esta norma reorganiza los límites a considerar para las clasificaciones ISO en cuanto al tamaño de las partículas.
Se eliminan los siguientes tamaños: el tamaño 0,2 µm de clase ISO 1, el tamaño 0,5 µm para ISO 2 y así sucesivamente hasta la ISO5 donde se elimina el tamaño 5 µm.
3.2. Controversia con el tamaño de 5µm
En este punto surge el primer conflicto con las normativas farmacéuticas que consideran el tamaño 5 µm como un elemento fundamental en la clasificación de zonas y procesos estériles.
El Anexo 1 de Estériles de la EU GMP recoge claramente este aspecto para los Grados A y B, tanto en reposo como en operación. Por otra parte, este mismo criterio del Anexo 1 ya ha sido adoptado por otras normativas internacionales como PIC/S, OMS (Anexo 6 Productos Estériles) y recientemente la GMP China.
Las características de esterilidad utilizadas en la industria Farmacéutica y biotecnológica son muy sensibles al tamaño de partícula mayor o igual 5 µm por dos motivos:
– Representa una alarma temprana sobre la posibilidad de un problema de contaminación.
– Los microorganismos en general tienen tamaños menores a 1 µm pero tienden a agruparse en parejas, cadenas o clusters formando unidades con tamaños mayores a 5 µm.
Sin embargo ha habido presión para conseguir suprimir estos tamaños de partículas con bajos límites de contaje.
Es de sobra conocido que los contadores de partículas pueden dar un pequeño número de contajes falsos debidos a ruido electrónico, luz desviada, coincidencia etc. Este aspecto esta incluso reconocido en el Anexo 1 Estériles EU GMP punto 13.
También se sabe que algunas partículas de tamaños mayores a 1 µm pueden ser interceptadas o detenidas en el interior de los tubos de captación si estos son demasiado largos (punto 6 del Anexo 1 Estériles EU GMP) con lo cual no llegarían a la óptica del contador o llegarían en momentos que no corresponden al muestreo del volumen de aire en el que estaban incluidas.
3.3. Solución acordada
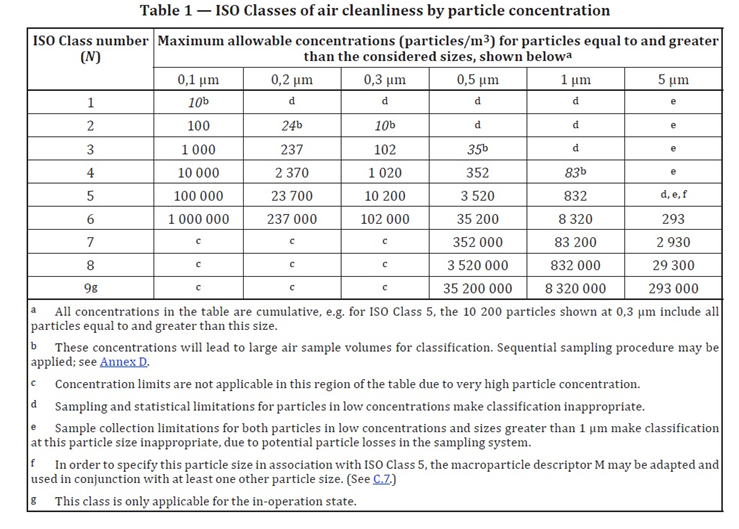
La solución acordada ha sido suprimir los tamaños con bajos números de contaje de la tabla, por lo que la ISO 5 solo llegará al tamaño 1 µm con el límite de 832 partículas; pero incluyendo expresamente una nota en la introducción dedicada a los productos estériles para el sector farmacéutico y afines, en la que se remite el caso de las partículas iguales o mayores a 5 µm a un nuevo anexo C (informativo, no normativo) dedicado a macropartículas.
Así mismo, en la tabla de clasificación ISO por concentración de partículas se ha añadido una nota (f) en el espacio dedicado al tamaño 5 µm en la línea de ISO 5, en la que se indica que para referirse a este tamaño de partículas en clasificación ISO 5 se debe utilizar el descriptor M del anexo C en conjunción con al menos otro tamaño de partícula.
Este nuevo anexo C es una evolución y ampliación del anexo E de la antigua edición en lo referente al descriptor M (macropartículas). El texto ha sido ampliado y completado con los tipos de equipos de medición posibles. De hecho la caracterización de la clase con el descriptor M requiere identificar no solamente el numero limite de partículas y su tamaño, sino también identificar el tipo de equipo de medición utilizado.
Un detalle importante es que en este nuevo anexo C se especifica que debe tenerse especial precaución con la longitud de los tubos que conducen la muestra desde la sonda isocinética hasta el contador para evitar la interceptación de partículas superiores a 1 µm. Aunque la norma se remite a las recomendaciones de los fabricantes de contadores, se recomienda distancias no superiores a 1m.)
3.4. Adaptación de la normativa farmacéutica
Ante esta situación la presión recae sobre las normativas farmacéuticas, fundamentalmente UE GMP en su Anexo 1 que también está en proceso de revisión y que previsiblemente aclarará la aplicación del tamaño 5 µm a los Grados A y B.
De hecho ya el Anexo 1 EU GMP define el Grado A como ISO 4.8 con límite de 20 partículas en el tamaño 5 µm. Aplicando la formula definida en ISO 14644-1 1999 a una ISO 4.8 le corresponderían 18 partículas de 5µ (no las 20 del Anexo 1) y 2.220 de 0,5 µm, sin embargo la tabla dada por el Anexo 1 especifica 3.520 partículas de 0,5 µm y 20 partículas de 5 µm.
Como curiosidad, con la ISO 14644 en la mano es imposible definir una clasificación ISO que dé el límite de 20 partículas para 5 µm. Habría que considerar una ISO 4.84 para lograr que la ecuación alcance el valor 20, pero la ISO excluye expresamente cualquier clasificación con más de un número decimal en su índice.
Por tanto es de esperar que el nuevo Anexo 1 de EU GMP conserve una tabla especifica de clasificación para los Grados A y B manteniendo la nueva ISO 14644-1 como norma de referencia para el resto de grados así como para la metodología y referencias.

Soporte Qualipharma
Puede contactar con Qualipharma para obtener más información sobre los cambios e impacto de la nueva normativa. Si lo desea también puede solicitar una formación in-company.
Auditorías GMP
La realización de auditorías bajo la normativa ISO 15378 son el método más fiable para valorar a un proveedor

1 comentarios
javier arango
muy buen articulo, esta norma es auditable y certificable?
Gracias