En la actualidad, a nivel europeo el marco normativo para la aprobación, dispensación y distribución del cannabis medicinal y sus derivados a los pacientes en los Estados miembros de la UE no está armonizado, por lo que existen distintas normativas nacionales.
En lo que respecta a la definición y categorización de la Flor de Cannabis, en el sentido más extenso de la palabra, de acuerdo con la monografía alemana de la flor de Cannabis publicada en 2017, “Cannabis flos”:
Las flores de cannabis consisten en el conjunto de las puntas de los brotes secos, florecidos, de la planta femenina de Cannabis sativa L. (Cannabaceae)
En función de su uso previsto, esta flor de Cannabis sativa L., tras ser procesada y tratada adecuadamente, puede convertirse en:
- Precursores para la extracción de APIs (Active Pharmaceutical Ingredient – Principio Activo Farmacéutico)
- Sustancia farmacéutica de origen vegetal
- Producto farmacéutico
- Medicamento a base de plantas
- Sustancia farmacéutica controlada
- Producto farmacéutico controlado
- Materia prima (de partida) para preparar medicamentos de fórmula (“magistral formula”) para el paciente
Cuando se habla de extractos, en lo que respecta a la clasificación en función de uso previsto, se atiende a las distintas etapas de los procesos de purificación a partir de los cuales pueden comercializarse, pudiendo tratarse de:
- Extracto Crudo
- Extracto Purificado
- Extractos estandarizados (añadiendo aislados de THC o CBD o mezclando extractos con diferentes contenidos de THC / CBD)
- Extractos preparados para consumo de paciente (ratio de THC/CBD estandarizado de acuerdo con las necesidades del paciente)
Sin embargo, ni el estatus ni la consideración de cada una de las tipologías de producto mencionados con anterioridad se encuentran armonizados, y los requerimientos regulatorios entre países y/o continentes presentan diferencias.
La no armonización existente en la UE relativa al cannabis medicinal y sus derivados afecta directamente a la fase final de procesado a partir de la cual se comercializan en los distintos Estados miembros de la UE. Entre otras, como se ha comentado anteriormente, se puede dar lugar a productos como flores secas, polvo, extractos u otras formas farmacéuticas. Incluso, se obtienen formas farmacéuticas finales que en muchas ocasiones pueden no estar cubiertas bajo la existencia de un Acuerdo de Reconocimiento Mutuo (Mutual Recognition Agreement, MRA) alguno, lo que añade dificultades en el proceso.
Aunque si bien es cierto que el cannabis medicinal y sus respectivos derivados se encuentran en la actualidad disponibles en algunos estados miembros de la UE como prescripción individual a pacientes sin necesidad de expedición de autorizaciones de comercialización convencionales; el marco normativo para la aprobación del cannabis medicinal y su distribución a los pacientes en los Estados miembros de la UE no se encuentra armonizado y existen distintas normativas nacionales. Por lo que, el actual marco regulatorio europeo existente para el cannabis medicinal y sus derivados se caracteriza por la no existencia de una definición precisa armonizada de los productos dispensados o a dispensar, ni de las condiciones en las que éstos se fabrican, registran y distribuyen.
En definitiva, ya se trate de productos tales como Cannabidiol, Extractos de Cannabis u otros cannabinoides, la falta de armonización afecta negativamente al correcto establecimiento de un mercado farmacéutico para el cannabis medicinal y sus derivados.
Las principales consecuencias derivadas de la no existencia de esta armonización pueden resumirse en las siguientes:
- Aplicación de legislación nacional adicional en los diferentes Estados miembros
- Diferentes puntos de partida para el comienzo de la aplicación de las BPF (Buenas Prácticas de Fabricación o GMP, Good Manufacturing Practices) de la UE
- Necesidad de registro o autorizaciones diferentes según el país destino de los productos
- Aplicación a diferentes requisitos de importación
Algunos países de la UE han encontrado ya la forma de facilitar la entrada de los productos de cannabis medicinal en sus mercados sin necesidad de que estos productos se encuentren sujetos a la concesión de una Autorización de Comercialización (MA, Marketing Authorisation) “tradicional”, concedida a los medicamentos, la cual requiere la realización de ensayos clínicos previos que demuestren la eficacia de éstos. Es el caso de Portugal donde la legislación actual permite la distinción entre los productos farmacéuticos y las sustancias o preparados a base de cannabis medicinal; requiriéndose para éstos últimos la concesión de una MA, por parte de INFARMED para su entrada al mercado, sin necesidad de realización de ensayos clínicos previos.
En Alemania también se ha facilitado la venta en farmacia de la flor de Cannabis en su envase final (incluyéndose el etiquetado), listo para el paciente sin requerirse la existencia de una Autorización de Comercialización (MA) y tradicional.
La flor de Cannabis se exportará a Alemania de tal manera que no exista ningún paso adicional entre las flores de cannabis secas y separadas obtenidas (API) y el envasado y etiquetado (final); quedando tan sólo un paso para llegar a ser un producto final. De esta manera, la flor a dispensar en farmacias será clasificada no como un producto final sino como una sustancia magistral para uso individual por paciente.
De estas diferencias existentes en cuanto a la clasificación de los productos a dispensar, también surgen diferencias en el punto de partida para el comienzo de aplicación de las BPF en cada caso.
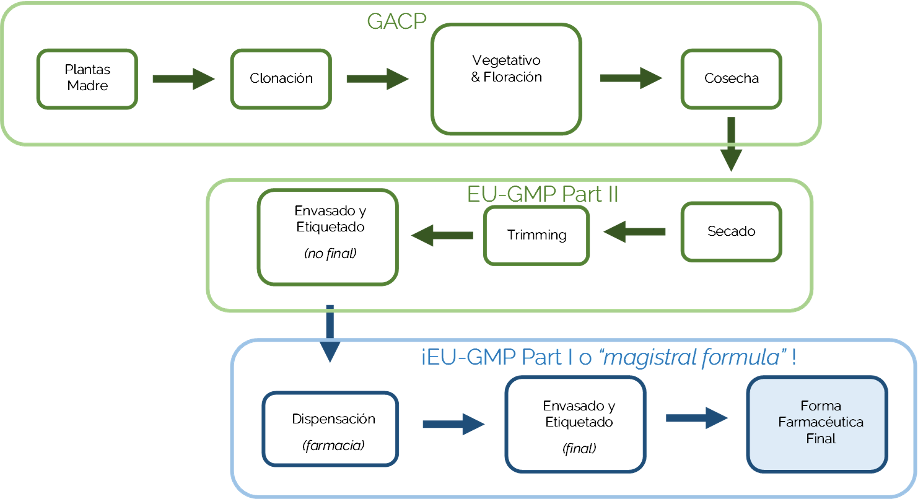
En la siguiente Figura se describe la aplicación de las diferentes normativas farmacéuticas al proceso de obtención de flores secas y separadas de Cannabis sativa L. Se describe para el caso de la regulación alemana explicada previamente:
De acuerdo con lo anterior, la aplicación de la normativa EU-GMP difiere en la última etapa del proceso para dar lugar a una forma farmacéutica final en función de la clasificación y categorización de este producto.
El mismo concepto de no armonización ha sido extendido en cuanto a la definición y establecimiento de los atributos críticos de la calidad de los productos con finalidad farmacéutica a base de cannabis medicinal. Las premisas generales en lo que respecta a este contexto hasta día de hoy y en la actualidad pueden resumirse como sigue:
- Hasta ahora no existen monografías armonizadas de la Ph. Eur. para la Flor de Cannabis o los Extractos de Cannabis
- Existen varias monografías nacionales sobre el cannabis
- Existen directrices sobre la calidad de los medicamentos a base de plantas (HMPs, Herbal Medicinal Products) dadas por el Comité de Medicamentos a base de Hierbas (HMPC, Comittee on Herbal Medicinal Products) de la EMA
Estableciéndose, entre otras muchas cuestiones, la necesidad de implementación de un sistema adecuado de garantía de calidad para la recolección y/o cultivo, la cosecha y el procesamiento primario de acuerdo con el cumplimiento de la normativa GACP (Good Agriculture and Collection Practices) europea. De esta forma, se alega a la obligatoriedad de existencia de una confirmación escrita de cumplimiento de GACP por parte del fabricante de la sustancia vegetal. También se referencia a los procedimientos de testeo adecuados y establecimiento de criterios de aceptación para sustancias y preparados vegetales, así como a Medicamentos a Base de Plantas de acuerdo a los capítulos correspondientes de la Ph. Eur.
El camino hacia la armonización para la definición y establecimiento de los atributos críticos de la calidad de los productos con finalidad farmacéutica a base de cannabis medicinal ha presentado avances en los últimos meses.
Ya fueron notificadas por el Comité de Medicamentos a base de plantas de la EMA, a través de su Plan de Trabajo y objetivos principales para el año 2022, tres nuevas monografías individuales de cannabis (1 para la flor y 2 para extractos) en trámite, que se encontrarán dentro del alcance de aplicación de la Ph. Eur.
Ante la presentación de este Plan de Trabajo se ha avanzado en el ejercicio de armonización de los atributos críticos de la calidad de los productos a base de cannabis medicinal en la UE, pues:
- El pasado mes de junio de 2022 fue publicado en Pharmaeuropa 34.3. un borrador de la monografía para CBD de la Eur., siendo la fecha límite para la realización de comentarios el 30 de septiembre de 2022.
- Este mes de octubre ha sido publicado el borrador de la flor de Cannabis en Pharmaeuropa 34.4. con un periodo de comentarios hasta el 31 de diciembre de 2022.
Además de las diferencias existentes en cuanto a la aplicación de la normativa en un marco de BPF de la UE, la falta de armonización también provoca que se han de tomar en cuenta diferentes normativas sobre “sustancias controladas / narcóticos” en los Estados miembros de la UE.
Generalmente, los productos a base de CBD con un contenido en THC inferior al 0,2 % no son considerados psicotrópicos. Sin embargo, Suiza cuenta con su propia normativa nacional sobre la consideración de “sustancias controladas / narcóticos” en relación a la cual los productos de CBD con contenido en THC inferior al 1 % no son considerados como narcóticos.
En Suiza ha sido implementada una guía general de aplicación titulada Products containing cannabidiol (CBD), en su cuarta versión actualizada en la que se incluye información sobre las distintas formas de ofrecer y distribuir materias primas y productos que contienen CBD, y acerca de su clasificación y comercialización en función de la situación legal actualizada. En base a la legislación vigente suiza se aclara que las flores de cáñamo que contienen menos del 1 % de THC, a pesar de no encontrarse sujetas a la ley de estupefacientes independientemente del nivel de contenido de CBD, no se pueden distribuir ni publicitar “a voluntad”. Esto es, dependiendo de la categoría del producto serán de aplicación la Ley de Productos Terapéuticos, la Ley de Alimentos o la Ley federal de Seguridad de los Productos, según convenga.
Con esta legislación y aclaración se restringe la publicidad o la venta de los productos que contienen CBD como terapéuticos en las tiendas al no encontrase aprobados como tal.
Puede concluirse, de acuerdo con lo expuesto a través del presente artículo que hoy en día aún hay mucho trabajo por delante a realizar por parte de las Autoridades Regulatorias en los diferentes países de la UE en cuanto a facilitar el comercio de los productos de cannabis medicinal y sus respectivos derivados de uso farmacéutico. Así, se hace estrictamente necesaria la definición precisa de estos productos como las condiciones de su fabricación, registro y distribución; no debiéndose definir solamente los productos desde un punto de vista de aplicación de la normativa EU-GMP, sino también atendiendo a la consolidación de normativas armonizadas europeas sobre la consideración de “sustancias controladas / narcóticas”.
Proyectos de Cannabis Medicinal
Mantente informado de los cambios en la regulación de cannabis medicinal en Europa y en el mundo